Wissenschaftler entdecken „molekularer Schalter“, der die Hirnentzündung bei Alzheimer antreibt
Ein neu identifizierter Auslöser für Hirnentzündungen könnte ein neuer Ansatzpunkt Verlangsamung Alzheimer-Progression sein.
Kurzfassung
Warum das wichtig ist
- Ein neu identifizierter Auslöser für Hirnentzündungen könnte ein neuer Ansatzpunkt Verlangsamung Alzheimer-Progression sein.
- Das Gehirn besitzt ein eigenes eingebautes Immunsystem, das Bedrohungen erkennt und darauf reagiert.
- Bei der Alzheimer-Krankheit zeigen wachsende Beweise, dass dieses System dauerhaft überaktiv wird.
Das Ergebnis ist eine chronische Entzündung, die die Verbindungen zwischen den Gehirnzellen schädigt. In einer präklinischen Studie mit menschlichen Alzheimer-Gehirnzellen haben Wissenschaftler öser hinter diesem Prozess identifiziert.
Die Entdeckung weist auf ein potenzielles Arzneimittelziel hin, das helfen könnte, die schädliche Entzündung zu kontrollieren. Ein molekularer Schalter hinter der Entzündung Die Studie, veröffentlicht in Cell Chemical Biology, konzentriert sich auf ein Protein namens STING.
Unter normalen Bedingungen fungiert STING als Teil des Frühwarnnetzwerks des Immunsystems. In Alzheimer-Gehirnen fanden Forscher jedoch heraus, dass STING eine chemische Veränderung namens S-Nitrosylierung (oder SNO, eine Reaktion, die Schwefel, Sauerstoff und Stickstoff beinhaltet) durchläuft.
Diese Modifikation treibt das Protein
Diese Modifikation treibt das Protein in einen überaktiven Zustand. Als Wissenschaftler diese Veränderung in einem Mausmodell blockierten, wurde die Hirnentzündung reduziert.
„Dies ist ein neues und wichtiges therapeutisches Ziel für die Alzheimer-Krankheit“, sagt der Hauptautor Stuart Lipton, Step Family Foundation Endowed Chair an Scripps Research und klinischer Neurologe.
„Es ist aufregend zu sehen, dass die Blockierung dieses Schalters bei Mäusen die Entzündung reduziert und die sehr neuronalen Verbindungen schützt, die bei Alzheimer verloren gehen, insbesondere weil wir den gleichen Signalweg in menschlichen Alzheimer-Gehirnproben und in menschlichen Stammzellen-Modellen aktiviert fanden.“ Vor über 30 Jahren beschrieb Lipton, der auch das Neurodegeneration New Medicines Center an Scripps Research mitdirektiert, erstmals die S-Nitrosylierung.
In diesem Prozess bindet ein Molekül,
In diesem Prozess bindet ein Molekül, das mit Stickoxid (NO) verwandt ist, an eine Cystein-Aminosäure in Proteinen und bildet „SNO“, wodurch sich das Verhalten des Proteins verändert. Das Labor von [Name des Labors fehlt] zeigte später, dass SNO durch Altern, Entzündungen und Umweltbelastungen wie Luftverschmutzung und Waldbrandrauch ausgelöst werden kann.
Diese Veränderungen können viele Proteine im gesamten Körper stören. Dieser weit verbreitete Effekt, bezeichnet als „SNO-STORM“, wurde mit Krankheiten wie Krebs, Parkinson-Krankheit und Alzheimer in Verbindung gebracht.
Das Schwachstelle Studie untersuchten die Forscher STING genauer, das bereits mit Alzheimer-bedingter Entzündung in Verbindung gebracht wurde.
Das Team , angeführt , arbeitete
Das Team , angeführt , arbeitete mit Professor John Yates III, einem Experten für Massenspektrometrie am Scripps Research und Inhaber des John Lytton Young Endowed Chair.
Sie identifizierten den genauen Ort, an dem die S-Nitrosylierung an STING stattfindet, und konzentrierten sich dabei auf eine einzelne Aminosäure, die als Cystein 148 bekannt ist. Wenn diese Stelle modifiziert wird, bilden STING-Moleküle Cluster und lösen eine entzündliche Signalgebung aus.
Erhöhte Spiegel dieser veränderten Form, genannt SNO-STING, wurden in postmortalem Hirngewebe , in im Labor gezüchteten menschlichen Hirn-Immunzellen, die Alzheimer-Proteine ausgesetzt waren, und bei Mäusen mit der Krankheit nachgewiesen.
Weitere Experimente zeigten, dass charakteristische Alzheimer-Protein-Aggregate,
Weitere Experimente zeigten, dass charakteristische Alzheimer-Protein-Aggregate, einschließlich Amyloid-beta und Alpha-Synuclein, die S-Nitrosylierung ösen können. Dies deutet auf einen Rückkopplungsmechanismus hin.
Proteinablagerungen, zusammen mit Alterung und Umweltstress, können Entzündungen auslösen, die Stickstoffmonoxid produzieren. Dieses wiederum modifiziert STING und verstärkt die Entzündung noch weiter.
Schutz der Hirnverbindungen Um diesen Mechanismus zu testen, erstellte das Team eine Version , der die Cystein 148 fehlt, was den Schritt der S-Nitrosylierung verhindert. Als dieses modifizierte Protein in ein Mausmodell der Alzheimer-Krankheit eingebracht wurde, reduzierte es die Entzündung in Hirn-Immunzellen signifikant.
Wichtig ist auch, dass es Synapsen,
Wichtig ist auch, dass es Synapsen, die Verbindungen zwischen Nervenzellen, welche für Gedächtnis und Denken unerlässlich sind, erhalten hat. Der Verlust Verfall bei Demenz verbunden, daher ist ihr Schutz ein Schlüsselziel in der Alzheimer-Forschung.
„Was dieses Ziel besonders vielversprechend macht, ist, dass wir die pathologische Überaktivierung dämpfen können, ohne die normale Immunantwort zu unterbinden“, sagt Lipton.
„Sie brauchen STING immer noch, um sich vor Infektionen zu schützen, und wenn wir Cystein 148 anvisieren, blockieren wir nicht das gesamte Molekül; wir verhindern lediglich, dass STING überaktiviert wird.“ Liptons Team entwickelt nun kleine Moleküle, die darauf ausgelegt sind, Cystein 148 zu blockieren, mit Plänen, diese in zukünftigen präklinischen Studien zu testen.
Quelle: „Redox regulation of neuroinflammatory pathways
Quelle: „Redox regulation of neuroinflammatory pathways contributes to damage in Alzheimer's disease brain“ , Piu Banerjee, Xu Zhang, Jazmin Navarro, Charlene K Raspur, Parth Patel, Tomohiro Nakamura, Emily Schahrer, Henry Scott, Nhi Lang, Jolene K.
Diedrich, Amanda J. Roberts, John R.
Yates and Stuart A. Lipton, 23 April 2026, Cell Chemical Biology.
DOI: 10.1016/j.chembiol.2026.03.017 Diese Arbeit wurde teilweise
DOI: 10.1016/j.chembiol.2026.03.017 Diese Arbeit wurde teilweise (R35 AG071734, U01 AG088679, RF1 AG057409, R01 AG078756, R01 AG056259, R01 DA048882, DP1 DA041722 und R01 AG077046) und dem U.S. Department of Defense/U.S.
Department of the Army (AR230101) unterstützt.
Thema weiterverfolgen
Quellenprofil
Quelle und redaktionelle Angaben
- Quelle
- SciTechDaily
- Originaltitel
- Scientists Discover “Molecular Switch” That Fuels Alzheimer’s Brain Inflammation
- Canonical
- https://scitechdaily.com/scientists-discover-molecular-switch-that-fuels-alzheimers-brain-inflammation/
- Quell-URL
- https://scitechdaily.com/scientists-discover-molecular-switch-that-fuels-alzheimers-brain-inflammation/
Aehnliche Inhalte
Verwandte Themen und interne Verlinkung
Weitere Artikel aus aehnlichen Themenfeldern, damit Leser direkt im selben Kontext weiterlesen koennen.
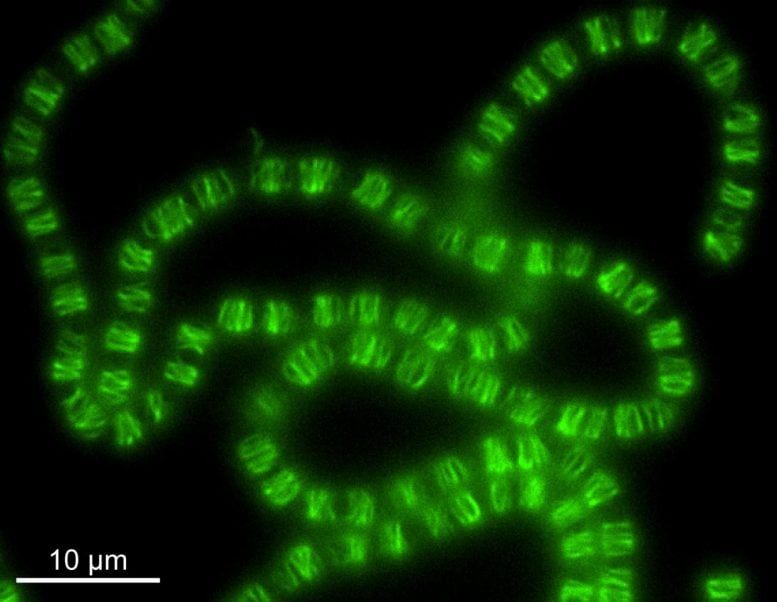
Uralte Bakterien verwandelten ein DNA-System in ein Zellgerüst
Ein System, das einst mit der DNA-Organisation Cyanobakterien verbunden war, hat sich zu einer Struktur entwickelt, die Zelle selbst formt.
28.04.2026
Live Redaktion
Forscher lösen nach 50 Jahren das Rätsel der Blutgruppen
Wissenschaftler haben eine verborgene Ebene Genregulation aufgedeckt, die hilft zu erklären, warum Individuen mit demselben Bluttyp auf molekularer Ebene so stark voneinander abweichen können.
28.04.2026
Live Redaktion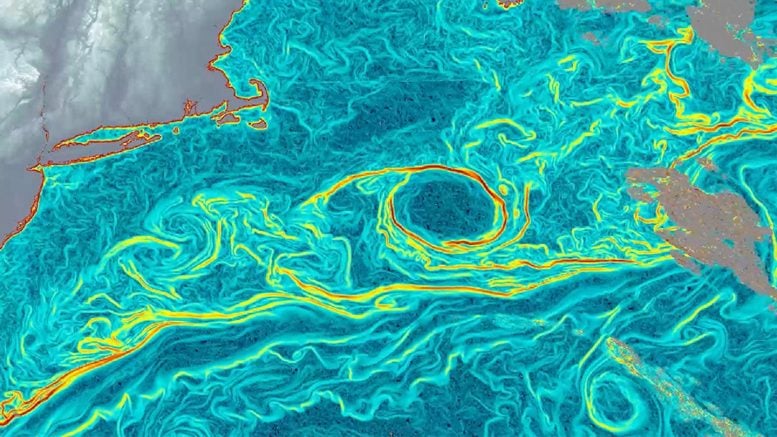
KI enthüllt verborgene Meeresströmungen in atemberaubender Detailgenauigkeit
KI verwandelt Wettersatelliten Echtzeit-Tracker der verborgenen Meeresströmungen.
28.04.2026
Live Redaktion
Bäume erzeugen während Stürmen winzige Blitzentladungen – Wissenschaftler haben es endlich bewiesen
Forscher haben den ersten realen Nachweis winziger elektrische Blitze erfasst, die Baumwipfeln während Gewittern leuchten.
28.04.2026
Live Redaktion